Highlight
| Intro | - 신소재공학과 염지현 교수팀, 카이랄 나노 소재 표면 처리 기술로 다양한 바이오 소재에 적용 가능한 나노 페인트 기술 개발 - 기존보다 4배 이상 향상되게 종양 조직을 괴사시키는 항암 온열 치료 기술 선보여 - 생명과학과 정현정 교수팀과 공동연구로 약물전달시스템에 적용하여 mRNA 치료제의 효율성을 극대화할 수 있는 새로운 패러다임 제시 - 약물 전달체, 바이오 센서, 촉매 등 다양한 분야에서 활용될 것으로 기대 |
|---|---|
| Principal Investigator | 염지현 교수 |
| Date | 2025-03-19 |
기존의 의료용 나노 소재는 체내에서 잘 전달되지 않거나 쉽게 분해되는 문제가 있었다. KAIST 연구진은 카이랄 나노 페인트 기술로 의료용 나노 소재에 카이랄성을 부여한 자성 나노 입자를 개발했다. 그 결과 항암 온열 치료 효과가 기존보다 4배 이상 향상됐고, 약물 전달 시스템에도 적용하여 코로나 19 백신 등 mRNA 치료제의 효율성을 극대화할 수 있는 새로운 패러다임을 제시했다.

(왼쪽부터) KAIST 신소재공학과 염지현 교수, 정욱진 석박사통합과정
KAIST(총장 이광형)는 신소재공학과 염지현 교수 연구팀이 바이오 나노 소재의 표면에 카이랄성*을 부여할 수 있는 ‘카이랄 나노 페인트’기술을 최초로 개발했고 후속 연구로 생명과학과 정현정 교수팀과 함께 mRNA를 전달하는 지질전달체** 표면에도 성공적으로 도입했다고 19일 밝혔다. 이 연구들은 각각 국제 학술지 ACS Nano와 ACS Applied Materials & Interfaces 에 게재됐다.
*카이랄성(Chirality): 카이랄성은 물체가 거울에 비친 모습과 겹치지 않는 성질을 의미함. 우리 몸에서도 카이랄성을 가진 분자들이 특정한 방식으로 작용하는데, 연구팀은 이를 활용해 나노 소재의 성능을 개선함
**지질전달체(Lipid Nanoparticle, LNP): mRNA, 유전자, 약물 등의 생체물질을 감싸서 세포 내부로 안전하게 전달하는 나노입자임. mRNA 백신(예: 코로나19 백신)과 같은 유전자 치료제에서 중요한 역할을 함.
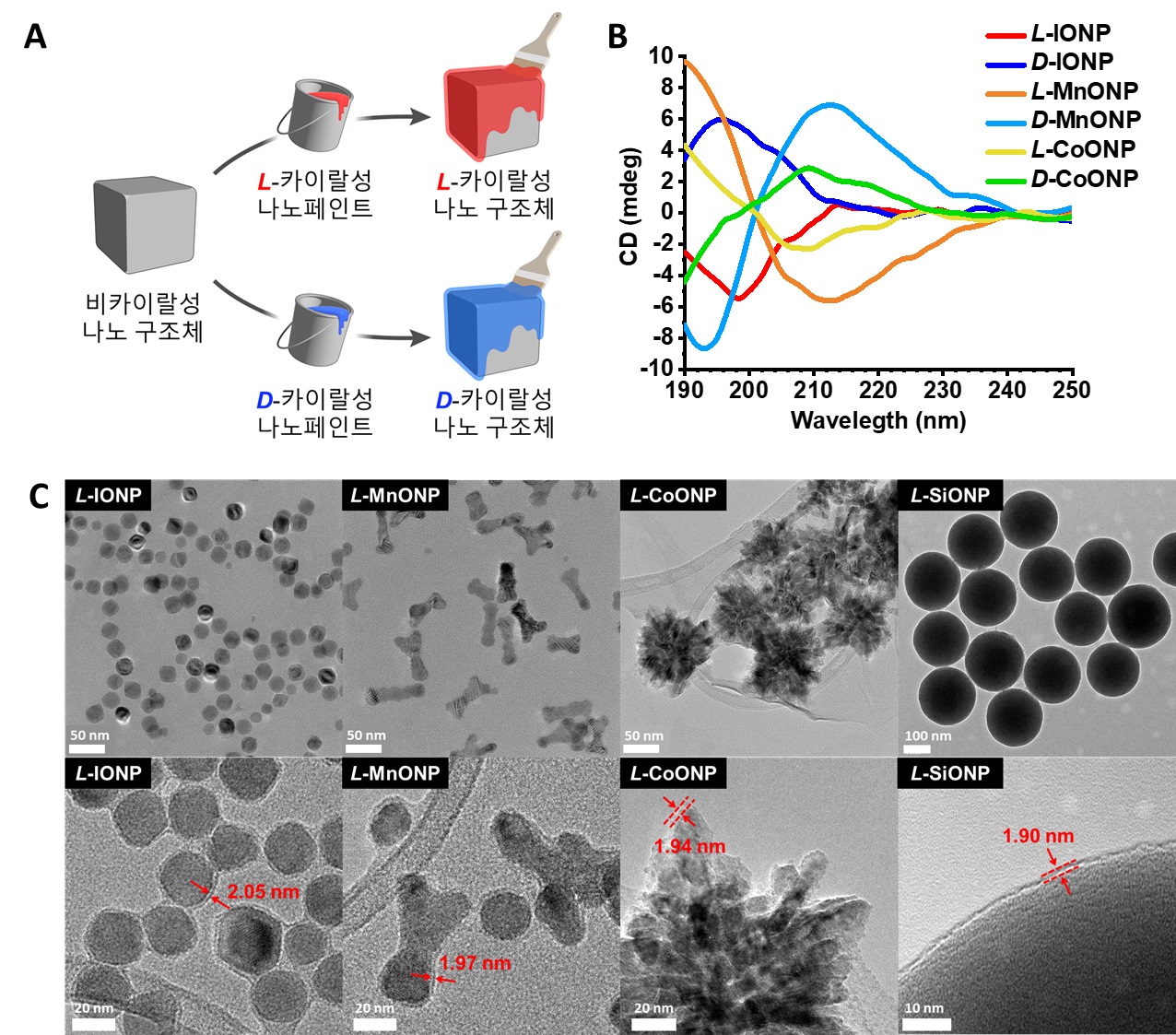
그림 1. A) 연구 모식도. 카이랄성이 없는 비카이랄 나노 구조체에 카이랄 나노 페인트를 적용하면 카이랄 나노 구조체를 얻을 수 있다. B) 카이랄 나노 페인트 기술을 통해 얻어진 카이랄 나노 소재의 원편광 이색성 분광 분석 결과. 두 그래프가 짝을 이뤄 상하 대칭을 이룸을 통해 얻어진 나노 소재가 카이랄성을 가짐을 확인할 수 있다. C) 카이랄 나노 소재의 전자 현미경 사진. 서로 다른 크기와 모양, 조성을 가졌으나 공통적으로 2 nm 두께의 카이랄 나노 페인트 층이 자리잡아 있음을 확인할 수 있다.
염지현 교수 연구팀은 우리 몸은 왼손잡이(L-형)와 오른손잡이(D-형) 구조를 가진 분자들이 서로 다르게 작용하는 카이랄 선택성(Chiral Selectivity)에 주목하고 나노 소재의 표면에 ‘카이랄 나노 페인트’를 적용해 카이랄성을 부여하는 기술을 개발했다. 이를 통해 십수 나노미터(nm) 크기의 작은 나노 입자부터 수 마이크로미터 (μm) 크기의 큰 마이크로 구조체까지 다양한 크기의 소재에 카이랄성을 입히는 데 성공했다.
연구팀은 더 나아가 카이랄 나노 페인트 기술을 활용해 카이랄 자성 나노 입자를 합성하고, 이를 종양에 주입한 뒤 자기장 처리로 생성되는 열을 통해 종양 조직을 괴사시키는 항암 온열 치료 기술을 선보였다.
이 과정에서 D-카이랄성을 가진 자성 나노 입자가 L-카이랄성을 가진 자성 나노 입자보다 암세포에 더 많이 흡수되고, 그 결과 4배 이상 향상된 항암 치료 효과가 있음을 증명했다.
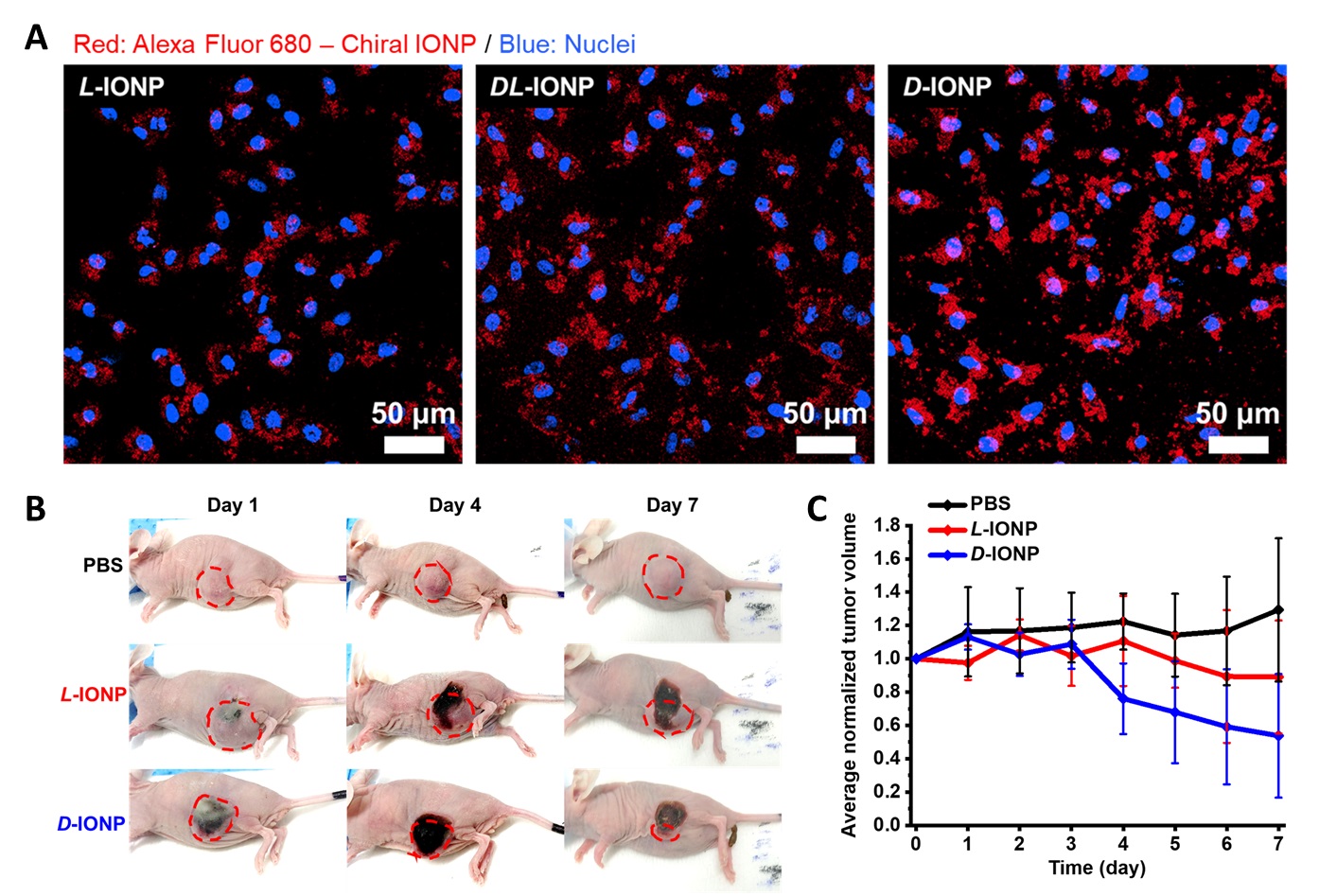
그림 2. A) 카이랄 나노 페인트 기술을 적용하여 얻어진 카이랄 자성 나노 입자를 암세포에 투입한 모습 (빨강: 카이랄 자성 나노 입자, 파랑: 암세포 세포핵). D-카이랄성을 가진 자성 나노 입자(D-IONP)가 L-카이랄성을 가진 자성 나노 입자(L-IONP)보다 더 많이 암세포 내부로 침투하였음을 확인할 수 있다. B, C) 카이랄 자성 나노 입자를 유방암 마우스 모델의 종양에 주입하고 자기장을 처리하여 항암 온열 치료를 한 결과. 항암 온열 치료를 실시하지 않은 대조군(PBS)은 종양의 크기가 증가한반면, L-카이랄성을 지닌 자성 나노 입자(L-IONP) 또는 D-카이랄성을 지닌 자성 나노 입자(D-IONP)를 활용하여 항암 온열 치료를 한 결과, 7일에 걸쳐 각각 11%, 46%의 종양 크기 감소 효과를 보였다.
이와 같은 암세포 내부로의 흡수 효율 및 항암 치료 효율의 차이가 나노 입자 표면에 처리된 카이랄 나노 페인트와 세포 표면의 수용체 간의 ‘카이랄 선택적 상호작용’에 의한 것임을 컴퓨터 시뮬레이션과 세포 실험을 통해 밝혔다.
향후, 카이랄 나노 페인트 기술은 의료용 바이오 소재를 비롯해 차세대 약물 전달 시스템, 바이오 센서, 촉매 및 나노 효소 등 다양한 분야에 응용될 것으로 기대된다.
신소재공학과 정욱진 석박사통합과정 학생이 제1 저자인 이번 연구 결과는 지난 3월 2일 국제 학술지 ‘에이씨에스 나노(ACS Nano)’에 온라인 게재됐다. (논문명: Universal Chiral Nanopaint for Metal Oxide Biomaterials) DOI: 10.1021/acsnano.4c14460
후속 연구로 mRNA를 전달하는 지질전달체 표면에 카이랄 페인트 기술을 도입했다. mRNA 기반 치료제는 세포 내에서 단백질을 직접 합성할 수 있도록 유전 정보를 전달하는 방식이지만, 전달체의 불안정성으로 인해 치료 효과가 제한적이었다.
카이랄 나노 페인트 기술은 이러한 문제를 해결하여 mRNA 치료제의 효율성을 극대화할 수 있는 새로운 패러다임을 제시했다. 그 결과, D-카이랄성 페인트를 도입한 지질전달체를 사용한 경우 mRNA의 세포 내 발현을 2배 이상 안정적으로 증가시켰다.
이 연구는 생명과학과 이주희 연구원과 신소재공학과 정욱진 박사과정 학생이 공동 1 저자로 국제 학술지 ‘에이씨에스 응용 재료 및 인터페이스(ACS Applied Materials & Interfaces)’에 3월 17일 게재됐다. (논문명: Chirality-controlled Lipid Nanoparticles for mRNA Delivery, DOI: https://doi.org/10.1021/acsami.5c00920)
염지현 교수는 “이번 연구를 통해 바이오 나노 소재의 성능을 크게 향상시키고 다양한 크기 및 모양을 가진 혁신적 나노 소재 합성 방법론을 제시했다. 앞으로는 이러한 카이랄 나노 소재를 활용해 암, 코로나 등 다양한 질병을 예방하는 백신부터 진단 및 치료하는 차세대 바이오 플랫폼 개발 및 연구를 지속할 계획”이라고 설명했다.
이번 연구는 과학기술정보통신부의 재원으로 범부처전주기의료기기연구개발사업단, 연구재단 우수신진사업 등의 지원을 받아 수행됐다.






